— В прошлое воскресенье вы передали результаты клинических исследований в Минздрав. Сами результаты пока не опубликованы. Расскажите об основных выводах этих исследований?
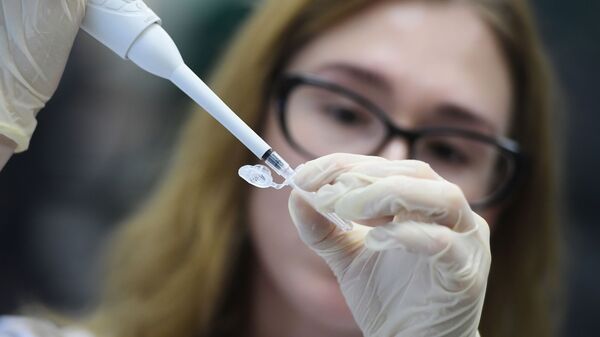
— Мы провели полный комплекс доклинических исследований безопасности и эффективности вакцины, а затем два клинических исследования, в которых вакцина изучалась с привлечением здоровых добровольцев по показателям безопасности и иммуногенности. Вакцина по результатам этих исследований показала хороший профиль безопасности и высокую иммуногенность.
У всех добровольцев, проиммунизированных нашей вакциной, были обнаружены вируснейтрализующие антитела и в случае применения сухой, и в случае применения жидкой форм вакцины. Также были проанализированы различные показатели клеточного иммунного ответа, в частности цитотоксические лимфоциты - очень важный параметр противовирусного иммунитета. Цитотоксические лимфоциты, которые удаляют из организма зараженные вирусом клетки, были обнаружены у всех вакцинированных добровольцев. Таким образом, по иммуногенности мы получили очень хорошие результаты.
По безопасности: ожидаемые нежелательные явления, которые выражались в виде температуры и боли в месте введения, наблюдались не у всех добровольцев. Но эти конкретные цифры будут опубликованы в ближайшее время.
— Какое количество людей приняло участие в испытаниях в первой и второй фазе?
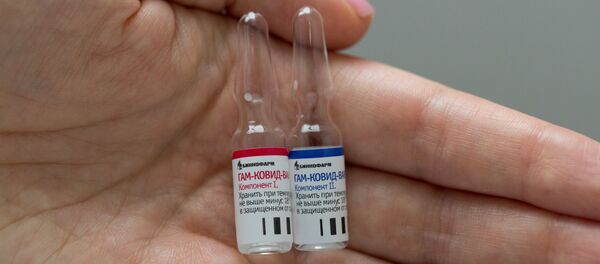
— В первой и второй фазе принимали участие 38 и 38 человек, то есть всего 76. Отличались два протокола тем, что вакцина по действующему веществу была одинаковая, но агрегатная форма была разная.
— А по возрасту насколько отличались участвовавшие?
— Добровольцы для первой и второй фазы набираются из возрастной группы 18-60 лет.
— В прессе часто повторяется утверждение, что на создание надежной безопасной вакцины нужно не меньше полутора лет. Могли бы Вы объяснить, как ученым Центра имени Н.Ф. Гамалеи удалось создать вакцину в столь короткие сроки, буквально за 5-6 месяцев?
— Неправильно говорить, что нам удалось создать вакцину "с нуля" за короткие сроки. Начиная с момента разработки технологии аденовирусных векторов до ее внедрения в практику прошло уже четыре десятка лет. С 2015 года вакцинами на основе аденовирусных векторов, разработанными в Центре им. Н.Ф. Гамалеи, было провакцинировано более 3 000 человек. Поэтому, это был не труд пяти месяцев, никоим образом.
Вакцины на основе аденовирусных векторов были созданы не только в России. Китай, компания CanSino, и Johnson & Johnson также работают с аденовирусными векторами. В первую очередь, это разработки вакцин против лихорадки Эбола. Эти платформы известны и хорошо изучены в рамках клинических испытаний.
Помимо результатов клинических испытаний в пользу безопасности данных платформ на основе аденовирусных векторов можно добавить то, что мы все болеем аденовирусами, и ни у кого никаких последствий в виде соматических заболеваний никогда не бывает.
У нас идет работа не с живыми аденовирусами, а с аденовирусными векторами, это вирусы, у которых удалены части геномов, и они не способны размножаться в клетках человека. Получается, что и с аденовирусами-то не страшно жить вместе, а с векторами, которые не способны размножаться, совсем безопасно. И мои слова подтверждаются десятками тысяч исследований этих векторов, в том числе множеством клинических исследований.
— Другие вакцины используют либо 26-й аденовирус, либо 5-й. А российская вакцина использует и тот, и другой. Вы можете более подробно объяснить, как это работает?
— Посмотрите на национальный календарь прививок, вы увидите, что очень многие вакцины бустируются. То есть, вы колете вакцину один раз, потом второй, третий и так далее. Для чего это делается? Для того, чтобы сформировать не только высокий иммунный ответ, но и чтобы этот ответ был пролонгированный, чтобы сформировать надежную иммуннологическую память.
Если не считать экономику, а заботиться о здравом смысле, длительности и уровне иммунного ответа, то стратегия прайм-буст иммунизации, то есть использование двух и более вакцинаций, всегда лучше. А делать прайм-буст вакцинацию разными векторами необходимо по простой причине: иммунный ответ после первого введения препарата будет формироваться в том числе и на вектор. Если вы будете вводить тот же самый вектор при второй иммунизации, то уже сформированный анти-векторный иммунитет будет снижать эффективность вакцинации. Поэтому, вы просто меняете вектор-носитель на тот, который иммунный ответ не распознает. Таким образом, вам удается незаметно для иммунной системы пронести нужный ген и сформировать иммунный ответ к целевому антигену.
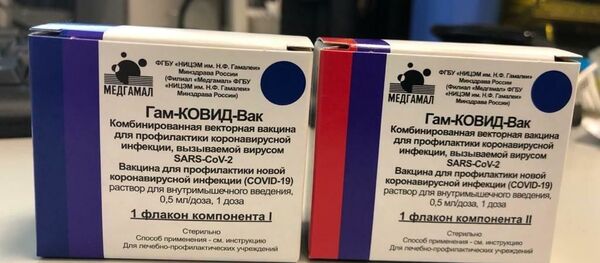
— Ваша вакцина получила временную регистрацию. Что это значит?
— Для чего временная регистрация существует? Мы же не здоровых добровольцев хотим с вами защищать последующие 1,5 года. Если мы работаем с обычным населением, среди которого есть группы риска, то есть люди, которые в результате перенесенной инфекции или станут инвалидами или погибнут, то нужен был механизм, который позволит на очень жестких условиях и ограничениях вывести вакцину в оборот в разумные сроки.
Что значит жесткие условия? Это значит, что каждая пробирка кодируется QR-кодом. Будет приложение для строго учета применения вакцины по всем стационарам и для учета всех нежелательных явлений у добровольцев. Каждый доброволец, который проходит вакцинацию, сможет сделать отчет о своем самочувствии в приложении.
Еще хочу подчеркнуть, что речь не идет о принудительной массовой вакцинации, решение о вакцинации каждый принимает для себя сам.
— Сейчас речь идет о каком примерно количестве людей, которые будут участвовать в третьей фазе?
— Окончательные цифры согласовываются, но я могу сказать, что исследования будут включать примерно 30-40 тысяч человек. Один из рабочих вариантов подразумевает, что 2 тыс. человек участвуют в клинических испытаниях по оценке параметров иммуногенности, а 28 тыс. добровольцев участвуют в наблюдательном исследовании для оценки эпидемиологической эффективности.
В настоящий момент мы еще дорабатываем протокол, чтобы он соответствовал всем нормам, в том числе международным.
— Чем отличаются друг от друга разные фазы клинических исследований?
— У нас в российском законе не прописаны понятия 1-й, 2-й, 3-й фазы. Это условное определение, которое используется в международной регуляторике. Первая фаза – это фаза оценки безопасности, ее редко проводят в чистом виде. В ней может участвовать 2-8-10-15, иногда 20 человек.
В условиях, когда исследуются вакцины, это довольно-таки глупая идея исследовать добровольцев только на безопасность и при этом не взять кровь и посмотреть тут же иммуногенность. Поэтому очень часто для вакцин классическую первую фазу делают совместно со 2-й фазой, на которой проходит оценка не только безопасности, но и эффективности. На этом этапе для вакцин эффективность оценивают по их иммуногенности. То есть на совмещенной 1-2 фазе вы определяете безопасность и иммуногенность по самым разным параметрам.
В ходе третьей фазы оценивается эпидемиологическая эффективность. Вы должны оценить, насколько провакцинированная когорта более защищена, чем невакцинированная когорта.
Хочу еще добавить, что к клиническим испытаниям нельзя приступать без успешного прохождения обязательной программы доклинических исследований. Это обширные исследования безопасности и иммуногенности на животных, без которых на людей переходить нельзя. И все параметры обязательно исследуются на большом количестве видов – грызуны, зайцеобразные, обезьяны. Все то, что, собственно, мы сделали перед тем как было принято решение приступать к клиническим исследованиям.
— Почему третья фаза исследований будет проводиться уже после временной регистрации?
— Идея и смысл временной регистрации в том, чтобы предоставить возможность доступа к вакцине группам риска и защитить тем самым людей от тяжелых последствий инфекции или гибели. При этом гражданский оборот вакцины будет осуществляться под жестким контролем, и эта временная регистрация может быть приостановлена в любой момент.
Целью третьей фазы является масштабная оценка безопасности и эффективности на большом количестве добровольцев в рамках контролируемого рандомизированного исследования. Это необходимо для получения большого объема статистических данных по всем параметрам испытаний. Кроме этого, этот этап необходим для принятия решения о постоянной регистрации вакцины.
— В ваш адрес звучала критика от представителей Всемирной Организации Здравоохранений (ВОЗ), которые говорили, что они не видели никаких научных исследований. Есть ли у вас какое-то взаимодействие с представителями ВОЗ?
— В принципе практика такова, что мы сначала предоставляем результаты экспертам Минздрава. Цель была получить безопасную и эффективную вакцину максимально быстро и это сделано, а потом уже переводить данные на английский язык и писать научные труды.
С одной стороны, это не отвлекает людей от поставленной задачи, с другой, это также не оказывает давления на экспертов, которые анализируют полученные нами данные. Когда мы публикуем что-то, то как-бы показываем, видите нас, мы опубликовали, нас цитруют и обсуждают - давайте нас регистрируйте. То есть решение публиковать данные после их рассмотрения Минздравом, позволяет провести непредвзятую экспертизу. Сейчас, когда мы зарегистрировали препарат, в ближайшие дни статья на английском языке будет подана в авторитетный международный журнал, она пройдет через экспертную оценку редакторов и рецензентов. Это не один-два дня, этот процесс должен занять какое-то время, но в любом случае весь материал собран, и мы подаем на публикацию. Надеюсь, что в ближайшее время у критиков не будет почвы.
— Как вы планируете увеличить производственные мощности?
— Ожидается, что массовое производство вакцины начнется в сентябре 2020 года. К концу 2020 года планируется довести производство вакцины до 200 миллионов доз, если задействовать все производственные площадки, включая международные
Для этого РФПИ финансирует запуск производства вакцины на базе производственных мощностей своих портфельных компаний Р-Фарм и Биннофарм, входящей в группу компаний Алиум.
Кроме этого, РФПИ сейчас видит огромный интерес к вакцине в мире и планирует провести независимую от российской 3-ю фазу клинических испытаний в разных странах, в том числе в Саудовской Аравии, ОАЭ, Бразилии и Филиппинах, а также начать массовое производство в ряде стран в партнерстве с локальными суверенными фондами, в том числе в Индии, Южной Корее и Бразилии. Дополнительно прорабатываются возможности производства вакцины в Саудовской Аравии, Турции и на Кубе.
Уже более 20 стран выразили заинтересованность в приобретении Спутник V, в том числе ОАЭ, Саудовская Аравия, Индонезия, Филиппины, Бразилия, Мексика и Индия.
— Ассоциация организаций по клиническим исследованиям (АОКИ) критиковала ученых Центра им. Н.Ф. Гамалеи за то, что они якобы вводили себе прототип своей же вакцины. По их словам, согласно международным стандартам, это является грубым нарушением. Как вы реагируете на эту критику?
— Ученые центра не пошли ни на какое нарушение. Ученые центра пошли бы на нарушение, если бы они стали ловить добровольцев на улице и без подписания информированного согласия и страховки вводить им вакцину. Вот это было бы как раз то, о чем говорили АОКИ, если бы мы так делали.
Поскольку разработчик имеет право ввести себе то, что он делает, и это не регулируется никак, вводили мы не потому, что мы – герои, хотим прославиться, а потому что люди просто работали в красной зоне, то есть с вирусом. Вся плазма больных коронавирусом в Москве проходила через нас, мы должны были контролировать активность этих плазм в отношении живого вируса, то есть наши сотрудники постоянно были под угрозой.
Более того, часть людей – немолодые, часть – с сопутствующими заболеваниями.
В общем, история простая - есть возможность защитить ближний круг, существует вакцина, которая создана на всесторонне изученной платформе и каждый из нас уверен в честности лично своих результатов и результатах коллег.
У нас много вакцин, созданных на этой технологической платформе, в том числе зарегистрированных, и никаких сюрпризов мы не ожидали. Мы, в первую очередь стремились защитить себя и ближний круг.
Хельсинская декларация также абсолютно не это регламентирует, она регламентирует порядок проведения клинических исследований. Мы не проводили клинические исследования в тот момент. То есть, все их претензии были бы обоснованы, если бы мы проводили клиническое исследование, собрали бы своих людей, вакцинировали и стали бы вносить это в досье о клинических исследованиях. Вот это, конечно, было бы нарушением. На самом деле, ничего этого не было, поэтому это просто дешевая подмена понятий.
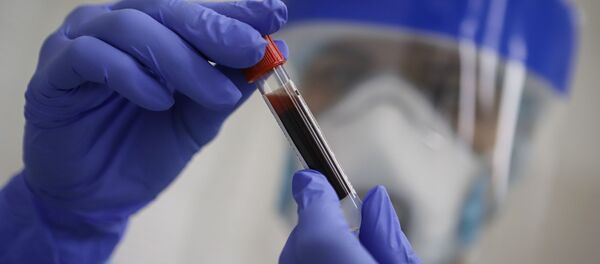
— Как соотносится уровень антител у тех, кто получил вакцину, и у тех, кто переболел коронавирусом, и что означает это соотношение?
— Во всем мире сейчас сравнивают уровни активности сыворотки у переболевших людей с уровнем активности у иммунизированных добровольцев.
Здесь довольно существенная разница в пользу вакцинированных потому, что при иммунизации нет интоксикации организма, нет тяжелого заболевания, поэтому ничего удивительного, что уровень антител выше у вакцинированных, чем у переболевших.
Мы уже знаем, что у очень многих переболевших людей антитела появляются, но потом держатся недолго, а с вакцинацией это гораздо более надежная история.
— Могут ли вашу вакцину получать люди, переболевшие коронавирусом? Возможны ли здесь какие-то нежелательные эффекты?
— Для меня в этом смысле нет абсолютно никаких проблем. Мы же ревакцинируемся каждый год от гриппа, при этом мы им болеем, никто не спрашивает, есть ли здесь проблема, можно на следующий год иммунизироваться, если в этом году болел гриппом.
Эти вопросы берут начало от пресловутого ADE-эффекта (Антителозависимое усиление инфекции — явление, при котором связывание вируса с не полностью нейтрализующими антителами вызывает его проникновение в иммунные клетки). Об этом явлении сейчас много говорят, но на самом деле, в отношении коронавирусов SARS и SARS-CoV-2 после вакцинации векторной вакциной такое усиление не происходит.
Если мы говорим о векторных вакцинах, то все вакцинированные выживают и не болеют, все невакцинированные животные умирают или имеют гораздо большие повреждения легких, чем вакцинированные.
Поэтому ни о каком ADE-эффекте в чистом виде, который бы конвертировался в усиление респираторного заболевания, в случае использования векторных вакцин речи не идет. Это не значит, что его не нужно изучать и смотреть.
Но на сегодняшний день эта история по поводу ADE сильно раздута. Эта история действительно существует в случае с вакциной против лихорадки Денге и других лихорадок. Но для коронавируса это не показано, им уже переболели миллионы людей, никаких случаев ADE-эффекта не нашли. Нету такого, чтобы переболевшие люди заболели еще раз и умерли, как с Денге.
На ADE-эффект нужно обращать внимание, нужно отслеживать, для всех вакцин, не только для коронавируса. Но говорить о том, что это гигантская проблема, и теперь есть ADE-эффект и из-за этого никогда не будет вакцины, это глупо. Я не видел ни одной доказательной научной статьи, которая бы рассказывала об этом.
— Во время создания российской вакцины, работали ли только российские ученые, или в создании вакцины принимали участие какие-то иностранные коллеги?
— Нет, конкретно эта вакцина разрабатывалась только в центре Гамалеи, ни с какими иностранными коллегами мы не сотрудничали.
Сама технология – это огромный пласт знаний и научного опыта работы. Естественно, с ней в мире работает очень много людей, есть масса публикаций, мы с этими публикациями знакомимся, они с нашими, это такое общее научное поле. Но непосредственно разработка вакцины, ее создание и масштабирование – это все велось только российскими учеными.